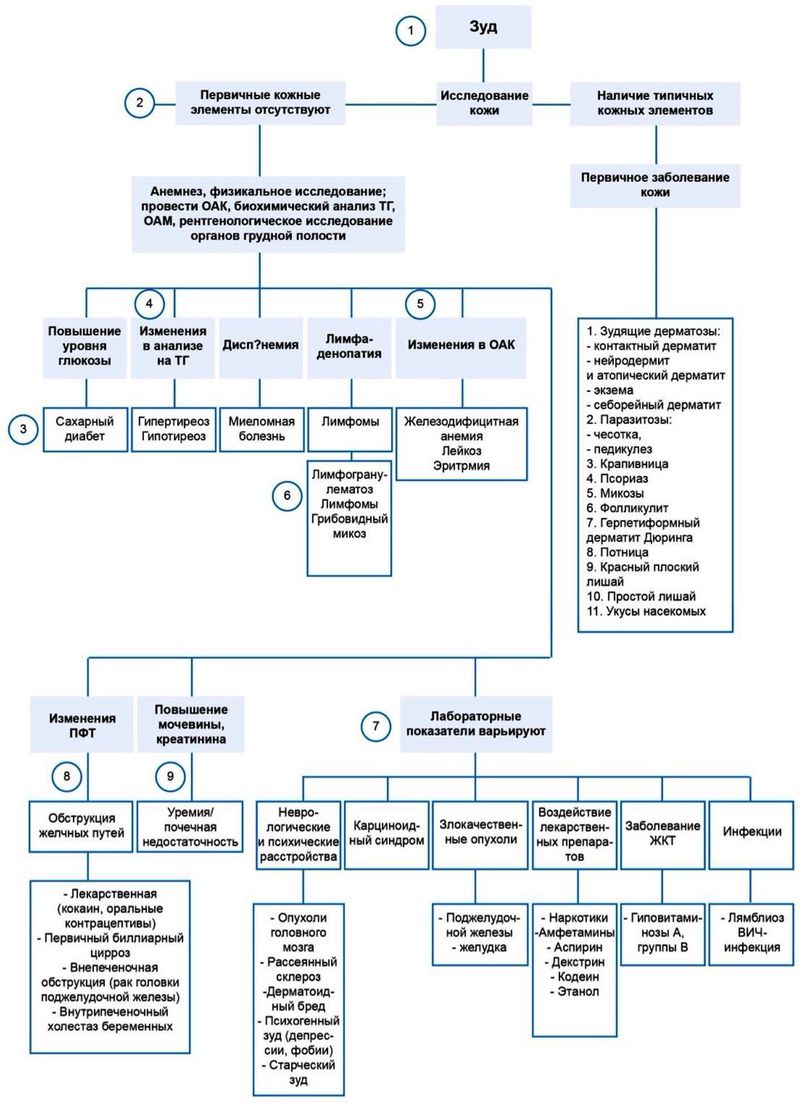
Предыдущий разговор закончился на том, что морфологические изменения структуры кожи, изменяя его качественные характеристики, могут становиться стимулом к изменению психики пациента… читать далее
Мутации в гене DES человека вызывают тяжелые миопатии и кардиомиопатии [1, 2]. Манифестация заболевания сильно варьирует и может быть с первого и до восьмого десятилетия жизни, причем сведения о доклинических стадиях заболевания крайне малочисленны. Ранние изменения в заболевании являются важной основой для будущих исследований, посвященных влиянию физических упражнений, а также фармакологических вмешательств.
Большинство наследственных миопатий клинически характеризуются прогрессирующей мышечной слабостью [3]. Постоянное нарушение цитоархитектуры скелетных мышц на уровне одного волокна может предшествовать и быть ответственным за прогрессирующую мышечную слабость.
При первично-мышечных заболеваниях морфологические исследования часто обнаруживают следующие изменения мышечных волокон, происходящие в случайном порядке: разнокалиберность размеров с развитием глубокой атрофии отдельных волокон или групп из нескольких близлежащих мышечных волокон, значимая гипертрофия отдельных волокон, продольное расщепление мышечных волокон, базофильные (регенерирующие) мышечные волокна [4].
Диагностика нервно-мышечных заболеваний представляет собой значительную сложность из-за выраженной клинико-генетической гетерогенности [5]. Одним из современных методов диагностики является МРТ мышц, позволяющий предположить, а впоследствии и подтвердить на генетическом уровне диагноз нервно-мышечного заболевания.
Цель исследования - изучение динамики клинической картины миофибриллярной миопатии с мутацией в гене DES c.1021A>C (Thr341Pro) в гетерозиготном состоянии и анализ родословной семьи.
Выявленная редкая форма миофибриллярной десмин-зависимой миопатии подтолкнула нас на исследование семьи пациента по линии отца (рис. 1) и подробного анализа течения заболевания у родственников.

Пробанд V:2 родился от второй беременности, первый ребенок (мальчик V:1) умер внутриутробно на 7 месяце беременности. Пробанд рос и развивался по возрасту, активно занимался спортом. В 30-летнем возрасте заметил спотыкания, слабость и усталость мышц, преимущественно нижних конечностей, трудность при подъеме по лестнице, нарушения сердечного ритма. Динамика результатов суточного мониторирования ЭКГ представлена в табл. 1. Неврологический статус пробанда в 33 года: тонус с рук не изменен, с ног снижен, сила в руках 5 баллов, в стопах обоих ног 5 баллов, в проксимальных отделах 3-4 балла, походка «утиная».

Эхокардиография (ЭХО-КГ) пробанда в 34 года: размеры полостей, толщина миокарда, работа клапанов не изменены; добавочная хорда в полости левого желудочка (ЛЖ), сократительная функция ЛЖ удовлетворительная.
В возрасте 35 лет пробанду по МРТ нижних конечностей был предположен клинический диагноз: миофибриллярная миопатия (десминопатия или αβ-кристаллинопатия). Затем методом прямого автоматического секвенирования проведено исследование образца ДНК пробанда и обнаружена замена c.1021A>C (Thr341Pro) в гене DES в гетерозиготном состоянии, мутаций в гене CRYAB не обнаружено. Далее проведена ДНК диагностика отца IV:1 пробанда и обнаружена аналогичная мутация; у сына VI:1 и матери IV:2 пробанда не обнаружена.
Неврологический статус пробанда в 38 лет: мышечная сила в верхних конечностях в левой кисти 4 балла, в правой 3 балла; в проксимальных отделах ног: сгибателях 1 балл, разгибателях 3 балла; мышечный тонус диффузно снижен, гипотрофия мышц плечевого пояса, грудной клетки, передней брюшной стенки, бедер; глубокие рефлексы с верхних конечностей живые симметричные, с нижних конечностей - коленные снижены, аххиловы отсутствуют; нарушений чувствительности нет; передвигается медленно с помощью трости, III группа инвалидности.
Отец IV:1 пробанда по окончании школы прошел двухлетнюю воинскую службу, требуемые физические нормативы успешно выполнял. Жалобы на слабость в ногах появились в возрасте 29 лет. Тогда при обследовании было установлено, что тонус мышц высокий, коленные рефлексы высокие, ахилловы отсутствуют, чувствительных расстройств нет, не может встать на носки и пятки, при ходьбе покачивается, курит с 18 лет. Предположен диагноз инфекционно-аллергический полирадиокулоневрит с нижним вялым парапарезом (стоп). В 30 лет слабость в ногах выросла, тонус снизился, атрофий не было, рефлексы снижены, основные функции сердца не нарушены. Через два года появилась гипостезия стоп и голеней с обеих сторон, причем стопы уже начали свисать. Данные биопсии мышц отца и пробанда представлены в табл. 2.

На фоне лечения отца пробанда отмечалось ухудшение состояния. Неврологический статус в 33 года: походка паретичная с высоким подъемом ноги так чтобы отвисающая стопа не цеплялась за опору, коленные рефлексы резко снижены, тонус в ногах снижен, брюшные реакции живые, лестничное вставание, сила в руках снижена до 3 баллов, больше слева, в ногах до 2 баллов, гипотрофия мышц обеих голеней, сухожильные рефлексы с рук снижены, гипостезия левой половины лица, на ногах по типу «чулок», на руках по типу «перчаток», передвигается с тростью, II группа инвалидности. В 34 года ошибочно выставлен диагноз спинальная мышечная атрофия. Динамика результатов игольчатой электромиографии (иЭМГ) членов семьи представлена в табл. 3.

С 41 года отец пробанда передвигался в инвалидном кресле, I группа инвалидности. Отмечалась выраженная гипотрофия дистальных отделов верхних и нижних конечностей, выраженный парез кистей – 1 балл, плегия стоп, нарушение функции тазовых органов по типу учащенного мочеиспускания. В следующем году перенес респираторный дистресс-синдром. Смерть отца пробанда наступила от легочно-сердечной недостаточности (пневмонии) в возрасте 49 лет через 20 лет после манифестации заболевания.
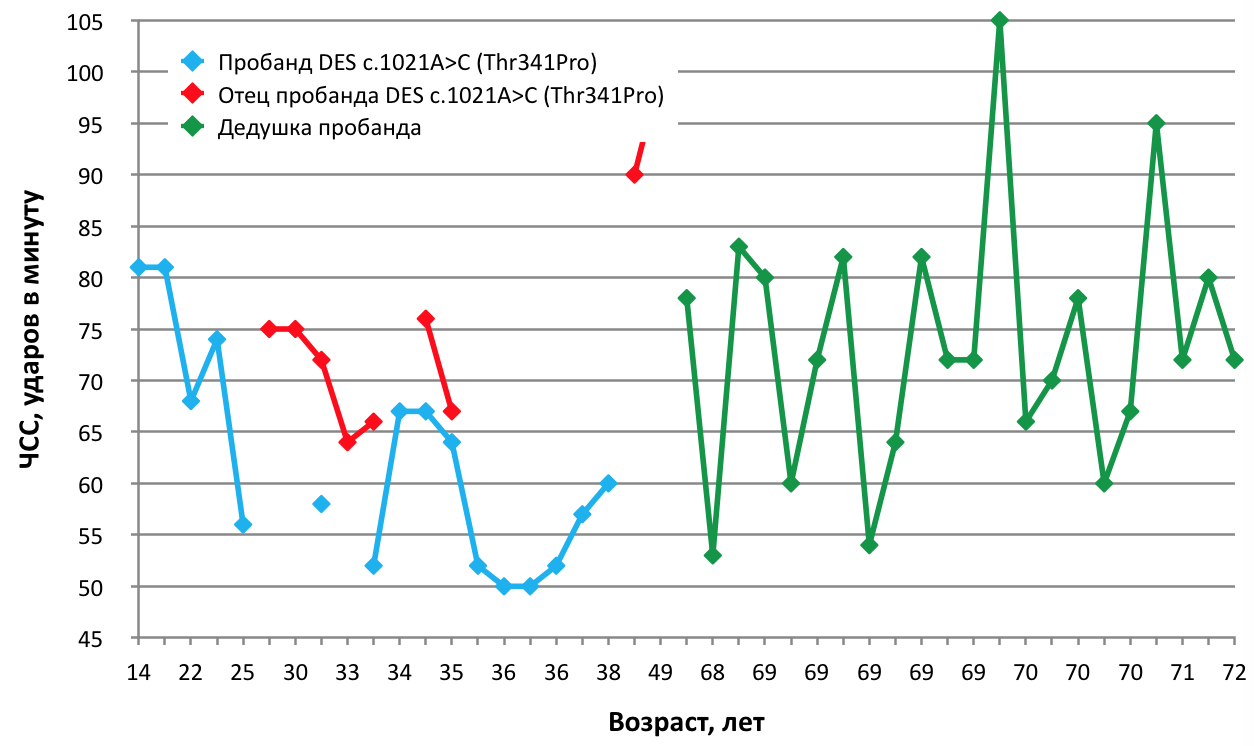
Дедушку III:1 пробанда с 35 лет периодически беспокоили боли в эпигастрии (хронический гастрит с пониженной секрецией). В 48 лет острый катаральный аппендицит, удален. В возрасте 46 лет перенес двухстороннюю пневмонию, в 61 и 62 года левостороннюю пневмониию. В 58 лет поставлен диагноз ишемическая болезнь сердца (ИБС). Динамика изменения частоты сердечных сокращений (ЧСС) членов семьи с десминопатией представлена на рис. 2. В 68 лет появилась одышка, уменьшающаяся в положении лежа, установлены стенокардия покоя и напряжения II функционального класса (ФК), признаки хронической коронарной недостаточности боковой стенки, атерокардиосклероз, IIА стадия недостаточности кровообращения.
В 69 лет у дедушки пробанда ночью произошел первый мелкоочаговый рецидивирующий передне-верхушечно-боковой с захватом перегородки инфаркт миокарда. В 70 лет второй инфаркт миокарда с последующей прогрессирующей стенокардией, постинфарктный кардиосклероз. В этом же возрасте обнаружена аденокарцинома прямой кишки II стадии (первые проявления в 67 лет). Проведен 1 этап внутриполостной гамма терапии на опухоль. Последующая ЭКГ сердца зарегистрировала синусовую тахикардию 95 ударов в минуту и обменные нарушения в миокарде. 2 этап прекратили после повторного приступа стенокардии с нарушением обменных процессов, гипоксией миокарда ЛЖ, признаками гипертрофии ЛЖ, диффузными дистрофическими изменениями. Дедушка пробанда умер в возрасте 72 лет от аденокарциномы прямой кишки.
Бабушка III:2 пробанда умерла в возрасте 88 лет от рака лимфоузлов. Старший родной брат III:3 дедушки пробанда умер в возрасте 66 лет от рака предстательной железы. У среднего родного брата III:4 дедушки пробанда был рак мочевого пузыря – скончался в 65 лет. Первый его ребенок IV:3 родился мертвым, второй сын IV:4 умер в 73 года в результате остановки сердца во сне. Родственники IV:6, IV:13, IV:20, V:18 умерли в результате несчастных случаев.
У старшей двоюродной сестры III:9 дедушки пробанда была ИБС, страдала одышкой, умерла в возрасте 78 лет от рака матки. Средняя двоюродная сестра III:11 дедушки пробанда умерла в возрасте 4 месяцев.
У младшей двоюродной сестры III:12 дедушки пробанда в связи с брадикардией, одышкой и АВ-блокадой III степени в 68 лет установлен электрокардиостимулятор (ЭКС). Однако ДНК диагностика не обнаружила у неё замены c.1021A>C (Thr341Pro) в гене DES, но возможно имелись другие мутации десмина. В 88 лет у неё была ИБС, стенокардия напряжения III ФК. ЭХО-КГ показала признаки атеросклероза аорты, кардиосклероза; незначительное снижение сократительной функции миокарда в покое (фракция выброса ЛЖ – 52%); дилатация левых отделов сердца и полости правого предсердия; недостаточность аортального клапана II степени, недостаточность трикуспидального клапана, лёгочная гипертензия. Скончалась в возрасте 88 лет от сердечной недостаточности.
Тетя II:4 дедушки пробанда умерла в возрасте 66 лет от инфаркта миокарда. Дядя II:3 дедушки пробанда скончался от рака мочевого пузыря в 74 года. Двоюродная бабушка I:4 дедушки пробанда умерла в результате сердечной недостаточности. У мамы II:2 дедушки пробанда в 80 лет был выявлен рак кожи - удалена опухоль, скончалась в возрасте 89 лет.
У сына VI:1 пробанда выявлен экзостоз, но результаты ДНК анализа не обнаружили мутации в генах EXT1, EXT2, причем данное заболевание отсутствует как у родственников пробанда, так и у родственников его супруги.
Анализ родословной семьи с десминопатией (рис. 1) показал, что в I и IV поколениях два родственника умерли в результате сердечной недостаточности. Во II и III поколениях 75 % членов семьи (9 человек) скончались от онкологических заболеваний и/или болезней сердца. Следует отметить, что дедушка пробанда и два его родных брата (100 % мужчин), умерли от рака соответственно в возрасте 72, 65 и 66 лет. В IV и V поколениях обнаружена мутация c.1021A>C (Thr341Pro) в гене DES у отца и пробанда. В VI поколении у сына пробанда выявлен экзостоз, что предполагает наличие у пробанда ещё других мутаций.
Проведенные исследования показали, что на доклинических стадиях и в начале заболевания у пробанда отмечалась желудочковая экстрасистолия (табл.1), которая к 38 годам исчезла, но появилась АВ-блокада и зарегистрированы патологические наджелудочковые аритмии. Характер изменения ЧСС у пробанда и его отца в одном возрастном интервале поразительно совпадает (рис. 2), но частота ударов у пробанда ниже (брадикардия). Биопсия мышц отца показала грубые структурные изменения (табл. 2), в отличие от биопсии пробанда. На начальных стадиях заболевания по иЭМГ (табл. 3) не регистрировалась спонтанная активность в мышцах отца (в 29 лет) и пробанда (до 33 лет), кроме того у последнего в 34,5 года исчезли единичные ПФЦ, регистрируемые ранее. Десминопатия прогрессирует у пробанда медленнее, чем у отца, с отсутствием гипостезии. Дедушка пробанда перенес два инфаркта миокарда в 69 и 70 лет, ИБС обнаружена также у его двоюродных сестер, причем у младшей в 68 лет был установлен ЭКС.
Вероятной причиной сердечной недостаточности у членов семьи могла быть изолированная десминовая кардиомиопатия. Кроме того, возможно мутация десмина способствует возникновению онкологических заболеваний, оказывая влияние на противоопухолевый иммунитет.
К сожалению, в рамках одной статьи раскрыть всю информацию о выявленном случае семейной формы миофибриллярной десмин-зависимой миопатии не получится, т.о. дальнейшие исследования будут представлены в следующих публикациях.
В связи с низкой распространенностью миофибриллярной десмин-зависимой миопатии в популяции диагностика данного заболевания представляет трудную задачу для врача-невролога. МРТ мышц с определением степени их повреждения позволяет предположить, а впоследствии и подтвердить на генетическом уровне диагноз нервно-мышечного заболевания. Проведенные исследования позволили выявить динамику клинической картины семейного случая миофибриллярной миопатии с мутацией в гене DES c.1021A>C (Thr341Pro) в гетерозиготном состоянии. Установлено, что причиной смерти родственников по линии отца пробанда в большинстве случаев становились онкологические заболевания и/или болезни сердца. Полученные данные могут быть в перспективе использованы для расширенных исследований неврологами, кардиологами, иммунологами, онкологами, генетиками с целью раскрытия механизма заболевания.

Предыдущий разговор закончился на том, что морфологические изменения структуры кожи, изменяя его качественные характеристики, могут становиться стимулом к изменению психики пациента… читать далее

Грешно на себя ссылаться, но как-то писал ранее, что человек (та ещё тварь) не стремится к добру или злу, а стремится к максимальному диапазону ощущений... читать далее
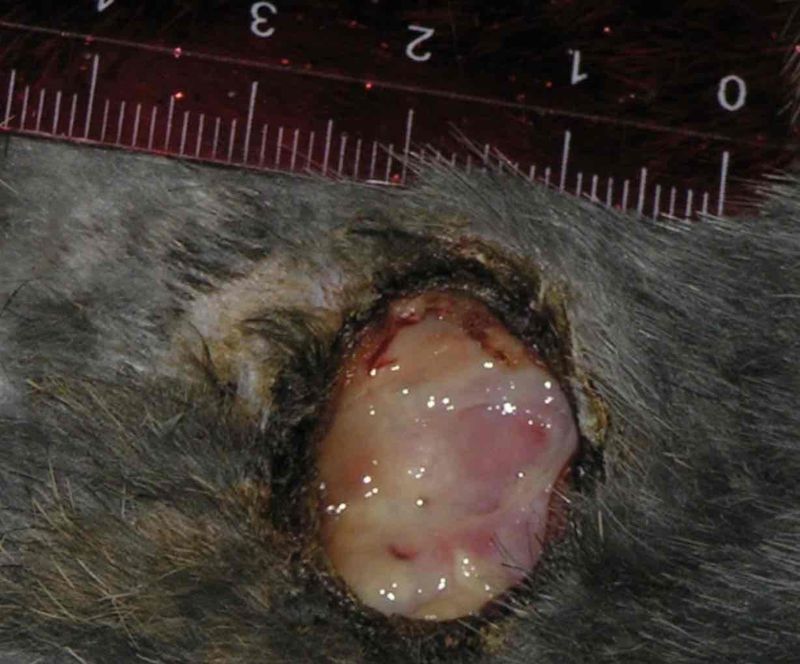
Необходимость в создании препаратов, обладающих одновременно антибактериальным и репаративным эффектом, остается актуальной... читать статью
Even to the horrors of war, the doctor gets used to much faster than an ordinary person, as well as soldiers, after two or three weeks already much without noticing and assessing what is happening, as a matter of course. What can we say about the events taking place during the expedition, when the phenomenon recorded by the photo may contain a different depth of meaning, often understood only after some time. The expedition Live Parallel, organized by Professor A. G. Teslinov in Peru and Bolivia and ended 2 months ago, was not an exception for me. Read more...